-
[기고] 말레이시아 의료기기 수출을 위한 규제제도 및 등록절차 – ②
- 외부전문가 기고
- 말레이시아
- 쿠알라룸푸르무역관 이주상
- 2019-08-07
- 출처 : KOTRA
-
- 의료기기 수출을 위해서는 규제체계 이해 및 사전 등록 필요 -
- ①편을 통해서는 규제체계 안내 ②편(이번 글)을 통해서는 등록 방법 안내 -
윤영균 법인장 메가젠임플란트(말레이시아)
의료기기 제품 등록 절차
A 등급의 의료기기는 현지 대리인(Authorized Representative)이 On-line으로 신청하면 되고 B, C, D등급은 적합성 평가기관 (CAB)에서 기술문서 심사를 먼저 받아야 한다. 외국의 의료기기 제조업체의 경우는 호주, 캐나다 EU, 일본, 미국 중 1개의 나라에서 받은 인증이 있으면 제품등록이 용이하다. 말레이시아에서는 의료기기 등록을 위해 제조공장 현지 검사가 필요하지 않으며, 일반적으로 임상 시험결과도 필요하지 않다.
의료기기 제품 등록 Process flow
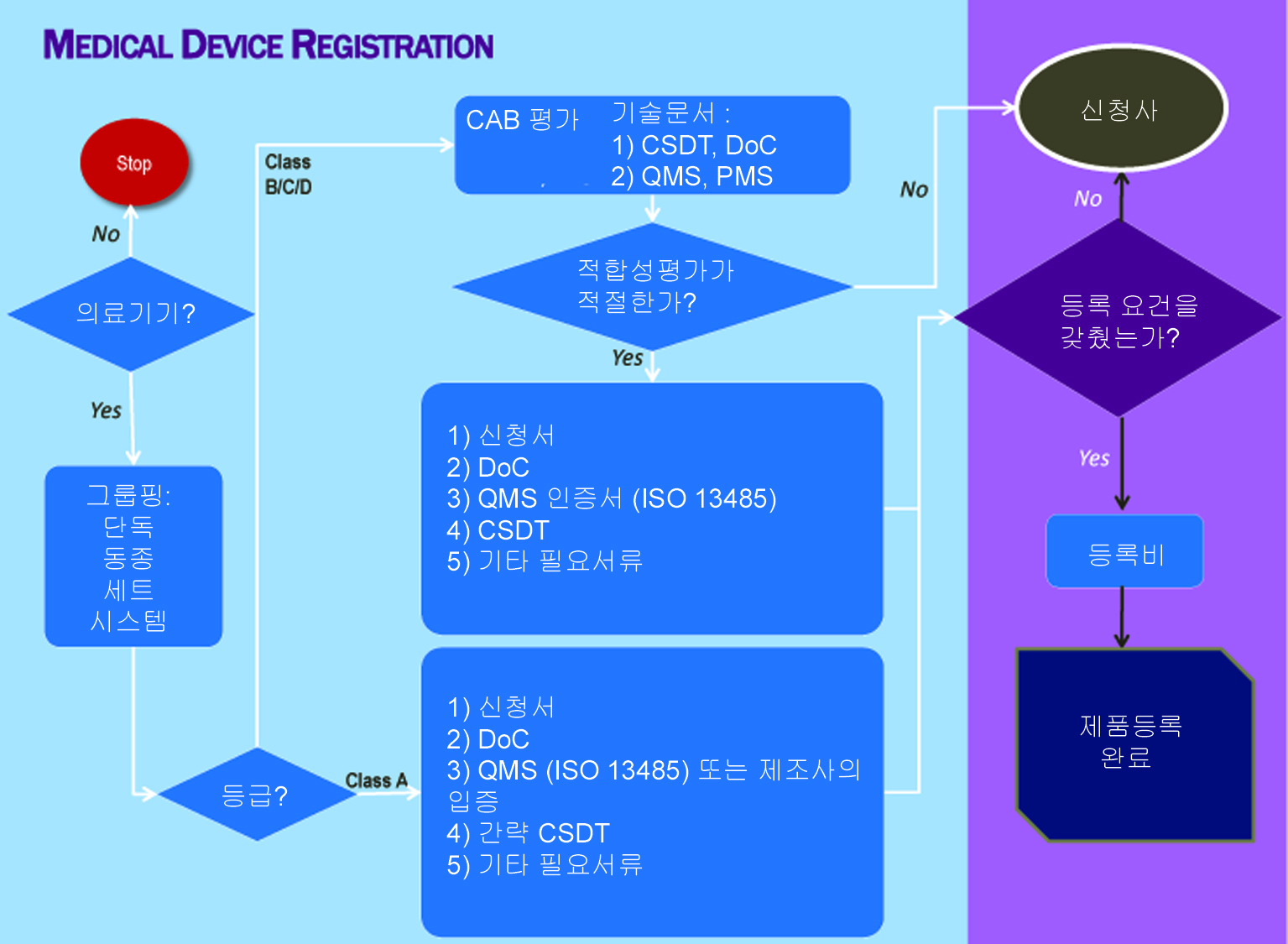
자료: 말레이시아 의료기기청, MDA
세부 등록 절차
Step 1: 의료기기 규정(Medical Device Regulations 2012)를 참조해 의료기기 등급을 확인한다. 말레이시아의 의료기기 등급은European Medical Devices Directive (MDD) 93/42/EEC와 유사하다.
Step 2: 말레이시아에 현지대리인이 없는 경우 말레이시아 내에 공인대리인(회사)(Authorized Representative)를 지정해야 한다. 제조회사는 제품군당 하나의 공인대리인(회사)만을 지정할 수 있다. 제품군이 다를 경우 별도의 AR을 지정할 수 있다. 제품등록은 AR이 실시한다.
Step 3: B, C, D 등급의 경우 공인된 적합성평가기관 (CAB)에 아세안 공통양식인 기술문서요약서 (CSDT : Common Submission Dissier Template) 형식을 사용하여 기술문서 심사를 받아야 한다. 제출문서는 CSDT외에 ISO 13485인증서, 라벨링, CE 인증서 등이 포함된다. A등급은 CAB의 기술문서 심사를 받지 않아도 된다.Step 4: CAB에서 기술문서 심사를 실시하고 증명서를 발급한다.
Step 5: 등록에 필요한 모든 문서(CSDT, CAB의 인증서, MDA신청서 등)를 준비한다.
Step 6: 말레이시아 AR통하여 MDA 의료기기 중앙집중식 온라인 시스템 (MeDC @ St)에 모든 자료를 업로드한다. 신청비용은 등급별로 차이가 있으며, 모든 서류는 영어로 제출하면 되나, 가정용 의료기기의 경우는 말레이시아어로 된 사용자매뉴얼과 라벨링이 필요하다.
Step 7: MDA 는 등급분류를 검증하고 신청서를 평가 한 후, 추가 문서보완 요청을 할 수도 있다. 문서 보완이 되지 않을 경우 신청서가 거부된다.
Step 8: 승인이 되면 등록번호가 기재된 증명서가 발급된다. 제품등록과 CAB인증서는 매5년마다 갱신하여야 한다.
Step 9: 말레이시아내의 AR은 지정대리인/수입자/판매대리점의 역할을 직접 수행할 수도 있고 별도의 수입자 또는 판매대리점을 지정할 수도 있다. 이 경우 AR은 허가서 (Authorization Letter)를 그 별도의 수입자 또는 판매대리점에게 발행해줘야 한다.제품등록 필요 서류
제품등록에 필요한 서류는 아래표와 같다.
제품등록 필요서류
준비서류
작성주체
1. Medical Device Authority Establishment Licence
1. 현지 지정 대리업체의 기관 라이선스
(Establishment License)
AR
2. Letter of Authorization from Manufacturer
2. 제조업체가 지정 대리인(업체)에 발행한 위임장
제조회사
3. Medical Device Grouping
3. 의료기기 그룹핑 목록
제조회사
4. QMS Certificate: -
4. 품질경영 시스템 인증서
제조회사
- ISO 13485 Certificate or Regulatory Authority Approval
- ISO 13485 인증 또는 규제 당국 승인
5. Post Market Surveillance: -
5. 사후시장 감시
제조회사
(i) Any incidents/Adverse incidents/FCA/Recall details
(ii) List of incidents for past 3 years
(iii) Date of last audit(i) 모든 사건/부정적 사건/FCA/리콜 세부 사항
(ii) 최근 3개년 사건 목록
(iii) 최근 감사일(iv) Declaration letter on post market surveillance from manufacturer(Appendix 4)
(iv) 사후 시장감시에 대한 자가 선언서
6. Technical Documentation: -
6. 기술문서
제조회사
(i) CE mark(certificate) or Letter/Certificate issued by Regulatory Authority
(i) CE 인증서 또는 규제당국에서 발행한 인증서
(ii) Label(individual device label)
(ii) 라벨(각 장비의 라벨)
(iii) CSDT(Please ensure that it is signed by the Manufacturer)
(iii) 기술문서요약서(CSDT)
(iv) Essential Principle of Safety and Performance(EPSP)
(iv) 안전과 성능관련 필수 원칙
7. Declaration of Conformity(DoC) per product as per MDA template.
7. 적합성 선언
제조회사
8. ATTESTATION BY APPLICANT FOR MEDICAL DEVICE REGISTRATION
8. 신청자의 입증서
AR
9. Cerificate of Conformity by CAB
9. CAB 적합성 평가서
CAB
자료: MedCert Malaysia Sdn Bhd
제품등록을 요약하면 아래와 같다.
제품등록 요약
No
구분
세부 내용
1
주무관청
의료기기청
Malaysian Medical Device Authority(MDA)2
관련규정
Act 737, Medical Device Act 2012
3
등급
Class A
Class B
Class C
Class D
4
등록경로
Class A
온라인 신청
Class B, C&D
CAB 심사+온라인 신청
5
지정대리인(회사)
말레이시아 내에 지정대리인(Authorized Representative)인 필요함
6
신청비용
Class A
RM100
Class B
RM250
Class C
RM500
Class D
RM750
7
품질관리시스템
ISO 13485
8
기술문서의 심사
Conformity Assessment Body(CAB)
9
유효기간
5년
10
라벨링
Schedule VI of Medical Device Rules 2012
11
제츨방식
12
최종 증명서
Registration Certificate
13
소요기간
1 - 9개월
14
문서작성 언어
영어
자료: 말레이시아 의료기기청, MDA
의료기기 제품 등록 비용
신청서, 등록료는 아래 표의 내용과 규정에 따라 다르다.의료기기 제품등록 비용
(단위: RM)
등급
신청료(RM)
등록료(RM)
A
100(25달러)
없음
B
250(63달러)
1,000(250달러)
C
500(125달러)
2,000(500달러)
D
750(188달러)
3,000(750달러)
의약품을 포함한 의료기기
없음
5,000(1250달러)
자료: 말레이시아 의료기기청, MDA
지정대리인(회사)의 변경
제품 판매실적이나 마케팅활동 부족 등 여러가지 이유로 지정대리인(Authorized Representative, AR)을 바꿔야 하는 경우가 생길 수 있다. 이 경우는 MEDICAL DEVICE GUIDANCE DOCUMENT, LICENSING FOR ESTABLISHMENT에 따라 적절한 절차에 의거 변경할 수 있다.
지정대리인 (Authorized Representative)의 변경
현AR
1. 현 지정대리인(AR)의 회사 서신에는 책임자가 서명해야 하며, 계약의 종료(termication)를 통보하는 내용이 담겨야 한다.
2. 의료기기 제조업체의 회사 양식으로 서신(Manufacturer’s Letter of Termination)을 위 AR의 서신과 함께 의료기기청(MDA)에 제출한다.신AR
신AR은 임명서(Letter of Authorization)와 함께 공식 회사 서신을 통해 AR의 변경을 의료기기청(MDA)에 통보해야 한다.
자료: 말레이시아 의료기기청(MDA)
제품등록증 샘플
제품등록이 완료되면 등록증과 별지(등록제품명 표기됨)로 구성된 인증서를 받는다. 등록증과 별지의 샘플은 첨부 파일을 참조하기 바란다.
등록제품의 조회
등록된 제품은 의료기기청(MDA) 웹사이트에서 조회가 가능하다. 아래 그림은 “콘택트렌즈”를 조회한 화면이다. 등록된 제품명과 등록번호, 등록자(Establishment) 그리고 등록기간을 조회할 수 있다.
등록제품의 조회(https://mmdr.mda.gov.my/data/public/index.php)
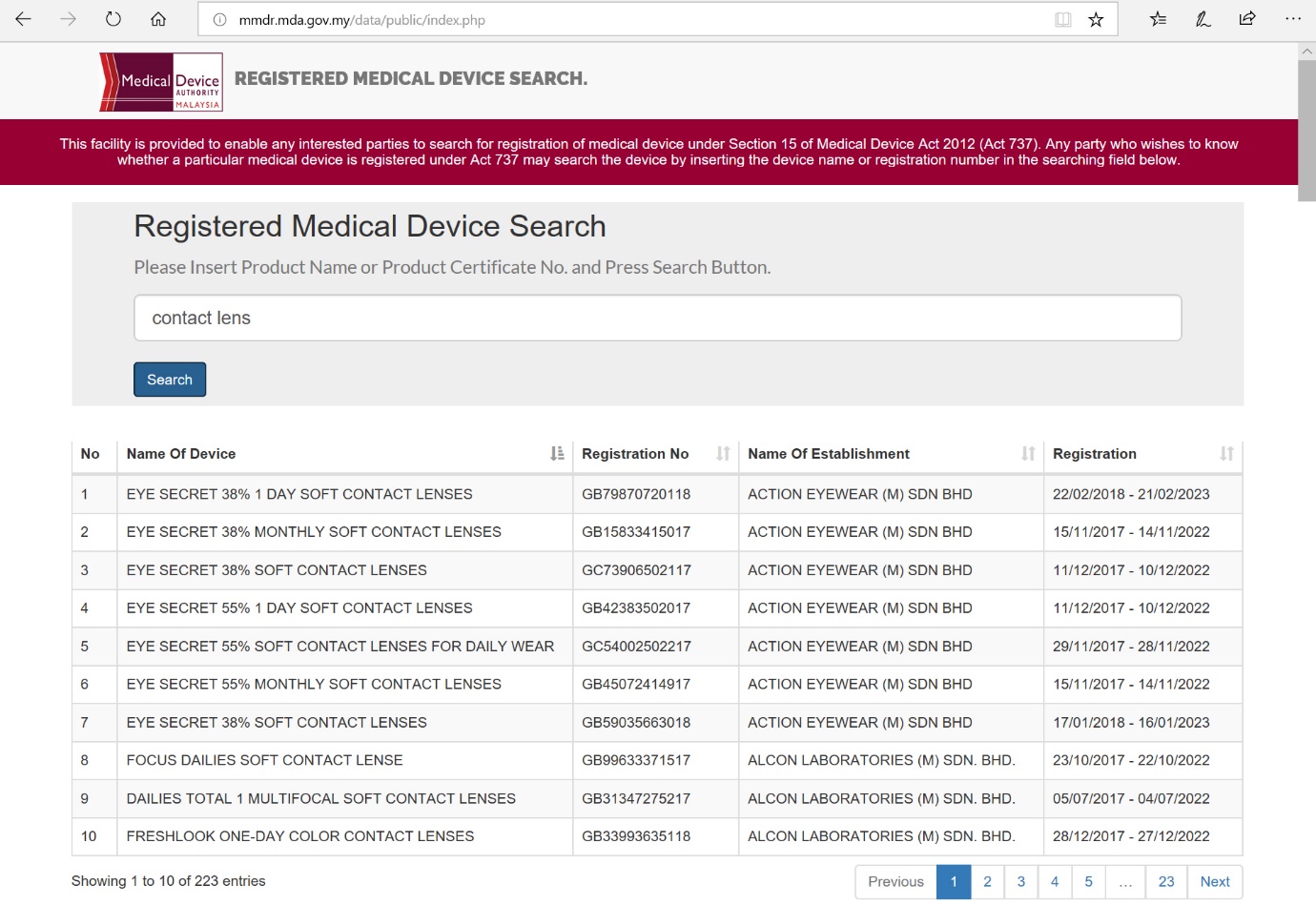
자료: 의료기기청(MDA)
기타, 방사선기기의 제품 등록
원자력 라이선스법(Atomic Energy Licencing Act 1984: AEL)에 의거해 X선 기기를 유통하고자 하는 회사는 원자력 에너지 허가위원회(Atomic Energy Licensing Board, AELB)로부터 클래스 C 라이선스를 받아야 한다. 또한 방사선기기를 말레이시아에 수입 또는 수출하려면 AELB 클래스 E 라이선스가 필요하다. 또한 방사선기기는 AELB에 별도의 제품 등록을 해야 한다.(MDA등록과는 별도임)
ㅇ 방사선기기정부 관련규제
방사선 관련 정부 라이선스의 종류
AELB라이선스의 종류
목적
신청양식
클라스 C
방사선기기의 판매 및 유통
LPTA/BP/3
클라스 E
방사선기기의 수입/수출
LPTA/BP/6
자료: 말레이시아 원자력에너지 허가위원회,AELB
위의 AELB 라이선스는 인터넷상의 ePermit으로 신청하고 및 실제 수입전에 취득해야 한다. 방사선기기 취급 라이선스 신청 방법 및 요약은 아래와 같다.
방사선기기 취급 라이선스 신청
신청서폼
LPTA/BP/3(클라스 C), LPTA/BP/ 6(클라스 E)
2부씩
심사료
각 15링깃
필요서류
회사소개서
방사선기기 소개서
방사선 탐지기 세부자료
필요인력
라이선스 관리책임자
1인
방사선안전관리사(Radiation Protection Officer, RPO)
1인
방사선 운영자
1인
필요장비
방사선 탐지기(Dose Meter)
최소2개
라이선스 비용
200링깃/클라스
자료: 말레이시아 원자력에너지 허가위원회(AELB)
방사선 안전관리사를 고용하지 못할 경우 방사선 방호 컨설턴트(Radiation Protection Consultant, RPC) 서비스를 최장 6개월까지 한시적으로 이용할 수 있다. 클래스 C와 클래스 E 라이선스는 동시에 신청할 수 있으며, 클래스 C 라이선스와 클래스 E 라이선스 취득 후 회사는 ePermit의 신청 수속을 수행할 수 있게 된다.
방사선기기 취급 라이선스를 획득 후 방사선 장비의 제품등록이 가능해진다. 방사선기기를 AELB에 등록하기 위해서는 아래와 같은 서류가 필요하다.
- CE 인증서
- 카탈로그
- 설치 매뉴얼
- 운영(사용자)매뉴얼
- 서비스 매뉴얼
- 기술도면
- 제조회사에서 발행한 현지 엔지니어 교육증명서
※ 해당 원고는 외부 전문가가 작성한 정보로, KOTRA 공식 의견이 아님을 알려드립니다.
<저작권자 : ⓒ KOTRA & KOTRA 해외시장뉴스>

KOTRA의 저작물인 ([기고] 말레이시아 의료기기 수출을 위한 규제제도 및 등록절차 – ②)의 경우 ‘공공누리 제4 유형: 출처표시+상업적 이용금지+변경금지’ 조건에 따라 이용할 수 있습니다. 다만, 사진, 이미지의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다.
-
1
[기고] 말레이시아 의료기기 수출을 위한 규제제도 및 등록절차 – ①
말레이시아 2019.07.26
-
1
대만 가정용 미용기기 시장동향
대만 2022-10-07
-
2
[기고] 말레이시아 의료기기 수출을 위한 규제제도 및 등록절차 – ①
말레이시아 2019-07-26
-
3
말레이시아 의료기기 등록 규정 및 절차 소개
말레이시아 2023-06-07
-
4
말레이시아 리튬이온 배터리 시장 동향
말레이시아 2019-10-11
-
5
2021년 말레이시아 의료기기 산업 정보
말레이시아 2022-01-13
-
6
호주의 가정용 미용기기 시장동향
호주 2021-10-28
-
1
2024년 말레이시아 스마트 농업 산업 정보
말레이시아 2024-04-09
-
2
2021년 말레이시아 ICT산업
말레이시아 2022-01-14
-
3
2021년 말레이시아 자동차 산업 정보
말레이시아 2022-01-13
-
4
2021년 말레이시아 신재생에너지 산업
말레이시아 2022-01-13
-
5
2021년 말레이시아 조선 및 선박 수리 산업 정보
말레이시아 2022-01-13
-
6
2021년 말레이시아 의료기기 산업 정보
말레이시아 2022-01-13













