-
인도 의료기기 인증 및 등록 절차
- 통상·규제
- 인도
- 뭄바이무역관 경기우
- 2020-04-10
- 출처 : KOTRA
-
- 2020년 4월 1일부 일부 의료기기에 한해 수입 절차 간소화 시행 -
- 관련 품목 인도 수출 희망 업체, 제품 위험 등급 확인 및 신청 요망 -
Make in India 정책으로 기존에 의료기기에 있어 70% 이상 수입에 의존하고 있던 인도는 2017년, 의료기기법(Medical Device Rules, 2017)을 도입해 2018년 1월부터 발효했고 모든 수입 의료기기에 대한 온라인 신청을 의무화시켰다. 이어서 2019년 10월 18일 인도 내 수요가 높은 일부 의료기기의 신속한 수입-유통을 위해 기존 의료기기법에 Chapter IIIA(Registration of Certain Medical Devices)조항을 추가하고 해당 조항은 2020년 4월 1일부터 의무화될 예정이다. 이에 의료기기 관련 우리 기업들은 사전에 수출 희망 품목 위험 등급 확인 및 수입 절차를 재차 확인할 것이 권고된다.
2017년 의료기기법(Medical Device Rules, 2017)
중앙의약품표준통제국(CDSCO)은 GHTF(Global Harmonization Task Force)에 따라 의료기기와 체외진단기기에 대한 분류 규정을 발표했다. 중앙의약품표준통제국의 산하기관인 CLA(Central Licensing Authority)는 관련 품목 분류표를 웹사이트에 공시하고 이를 관리하고 있다. 2019년 5월 기준 2017 의료기기법(Medical Device Rules, 2017)에 근거해 395대의 의료기기와 247대의 체외 진단 의료기기가 적용되고 있다.
위험군별 분류 목록(2019년 5월)
분류등급
위험성
예시
Class A
저위험군
카테터, 봉합제, 알코올 솜, 탈지면 등
Class B
저-중위험군
정맥 내카테터, 소독약, 골수 세포 분리기, 디지털 온습도계, 혈압 모니터링 기기, 흡인 바늘 등
Class C
중-고위험군
골시멘트, 분기 스텐트, CT 스캔 장비, MRI 장비, 투석기 등
Class D
고위험군
코퍼 티(Copper T), 심근패치, 흡장 카테터, 경동맥 스텐트, 디스코 인공보철물, 인공와우 이식기 등
자료: 중앙의약품표준통제국(CDSCO)
2017년 의료기기법 대상품목 예시
의료기기
체외진단기기
애블레이션
인공심장판막
임상용 시약 키트
암 진단용 시약 키트
외과용 골시멘트
체내 인공기관 대체물
혈액 검사 키트
혈액응고 검사 키트
심장스텐트
인공수정체
소변 검사 키트
약물 수준 평가 키트
카텐터
IV 캐뉼라
자가 진단 의료 키트
자가면역장애 진단 키트
피임약
정형외과 임플란트
현장진료검사 키트
선천성 질환 진단 키트
소독약
스칼프베인세트
ToRCH 진단 키트
심장 마커 진단 키트
일회용 피하 주사기
봉합제
감염 방지 키트
유전자 검출 키트
일화용 피하 흡입기
CT 스캔 장비
성염색체 검출 키트
혈액형 검사기
일회용 관류 세트
MRI 스캔 장비
항체 검출 키트
글루코미터
약물 용출 스텐트
세동 제거기
신장 투석기
PET 장비
X-Ray 기기
골수 채취기
의료용 분무기
혈압 모니터
디지털 온도계
장기 보존 솔루션
혈액 주머니
자료: 중앙의약품표준통제국(CDSCO)
인도 의료기기 온라인 수입 신청
모든 수입 의료기기는 CDSCO가 운영하는 의료기기 온라인 접수처(SUGAM)에 수입 신청을 해야 한다. CDSCO는 수입 허가된 자에 한해 등록 번호를 부여하며, 해당 번호는 수입업자가 의료기기 라벨 부착 시 기재돼야 한다. 2019년 10월 18일 중앙의약품표준통제국(CDSCO)은 인도 내 수요가 높은 일부 의료기기에 대한 수입 절차를 간소화하기 위해 2017년 의료기기 법(Medical Device Rules, 2017)에 특정 의료기기 등록 절차 관련 사항(Chapter IIIA: Registration of Certain Medical Devices)을 추가했다. 해당 조항은 2020년 4월 1일부터 발효되며, 18개월 동안 자발적으로 이뤄진다. 기기 목록과 온라인 신청 시 필요한 정보로는 1. 수입처 회사(기관)명, 2. 사양 및 표준 규격, 3. 세부 정보(모델명, 시리얼번호, 용도, 위험등급, 기대수명, 멸균상태, 브랜드명), 4. 국제인정기구포럼(IAF) 적합증명서, 5. 원산지 자유판매증명서, 6. 신청자에 대한 수입업체 확인 성명서 등이 있다.
수입 신청 절차 간소화 대상 품목 예시
일회용 피하 주사기
옵티컬 렌즈
애뷸레이션
혈액 주머니
CT 스캔 장비
(2021년 4월 1일부 유효)
일회용 피하 니들
정맥주사
혈관 봉합용
스테이플러
장기 보존 솔루션
MRI 장비
(2021년 4월 1일부 유효)
일회용 관류 세트
외과용 골시멘트
자궁내 장치(Cu-T)
네블라이저
(2021년 1월 1일부 유효)
제세동기
(2021년 4월 1일부 유효)
면역 혈청 진단 키트
심장 인공판막
콘돔
혈압 모니터
(2021년 1월 1일부로 유효)
PET 장비
(2021년 4월 1일부 유효)
심장 스텐트
스칼프 베인 세트
나팔관 링
포도당 측정기
(2021년 1월 1일부 유효)
X레이기기
(2021년 4월 1일부 유효)
약물 용출 스텐트
정형외과용 임플란트
봉합제
디지털 온도계
(2021년 1월 1일부 유효)
투석용 기기
(2021년 4월 1일부 유효)
카테터
체내 인공기관 대체물
U-테이프
임플란트 의료기기 장비들
(2021년 4월 1일부 유효)
골수 채취기
(2021년 4월 1일부 유효)
소독제 및 살충제
초음파장비
(2020년 11월 1일 부 유효)
자료: 중앙의약품표준통제국(CDSCO)
수입 신청 절차 시 인도 내 대행업체(기관) 필요
인도 내 규정상 해외 제조업체 및 공급업체는 의료기기 수출 시 수입 신청 절차를 대행해 줄 업체(기관)가 필요하다. 대행업체의 경우 현지 시장에서 의료기기를 판매할 수 있는 취급허가증을 소지해야 하며, 신청서를 작성해 인도 보건가족복지부(MoHFW) 웹사이트에 제출해 수입허가 신청을 해야 한다. 해당 절차는 위험 등급 분류에 상관없이 모든 품목에 대해 동일하며, 대행업체(기관) 변경 신청은 수입 허가 이후 180일 이내에만 가능하다. 2022년부터 판매, 유통용 수입 의료기기는 DI(Device Identifier)와 PI(Production Identifier)를 포함해야 한다.
웹사이트 예시
자료: 중앙의약품표준통제국(CDSCO)
의료기기 인증 취득 절차
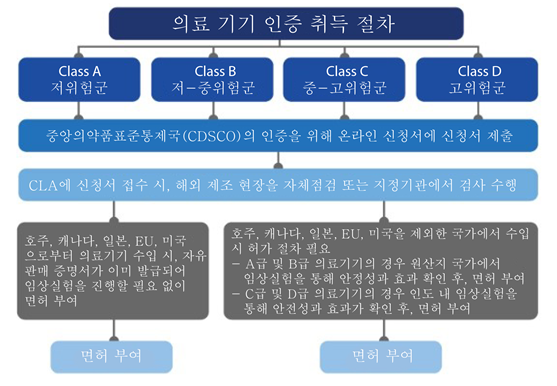
자료: 중앙의약품표준통제국(CDSCO)
수입 허가 절차
대행기관(업체)을 통해 CLA(Central Licensing Authority)에 신청서 접수 시 제조현장에 대한 자체심사 또는 지정기관 심사를 받게 되며, 심사비용은 신청자가 지불해야 한다. CLA는 신청서, 제출서류, 점검보고서 등을 검토 후 허가증을 부여한다. 절차 소요시간은 신청일로부터 9개월 이내이다. 반려된 경우 신청자는 45일 이내에 재심의 신청이 가능하다. 해당 허가는 영구적이며, 취소되지 않는 한 계속 유효하다. 허가소지자는 5년마다 규정된 허가유지 수수료를 지불해야 하며, 연체료 지불 시 90일까지 납부 연기가 가능하다. 그러나 기간 내 허가유지 수수료 미납 시 면허 취소로 간주되며, 허가 필요 시 신규 신청해야 한다.
자유 판매 증명서
호주, 캐나다, 일본, EU, 미국을 제외한 나머지 국가들로부터 의료기기 수입 시 자유 판매 증명서를 발급받아 수입 허가증 신청 시 제출해야 한다. 위험군 Class C 및 D의 경우 인도 내 임상실험을 통해 안전성과 효과가 확인 후, 판매 증명서가 발급된다. 저 위험군인 Class A 및 B의 경우에는 안전성과 효과 확인을 위한 임상실험을 원산지 국가에서 실시하며, 해당 결과를 근거로 판매 증명서가 발급된다.수입 허가 비용
등급별 취득 비용
(단위: 달러)
등급
기본 비용
품목 개수별 비용
Class A
1,000
50
Class B
2,000
1,000
Class C&D
3,000
1,500
Inspection of the overseas manufacturing site
6,000 이상
예시) Class A 제품 면허 취득 시, 해당 카테고리 세부 품목 구분이 5개일 경우,
1,000(기본비용)+50x5(개수별 비용)=1,250
자료: 중앙의약품표준통제국(CDSCO)
의료기기 라벨링
의료기기 라벨에는 의료기기명, 제조사명 및 제조사 주소, 무게, 길이, 부피, 개수, 제조연월 및 사용기한 등의 세부정보가 포함돼야 한다.
지정양식 예시
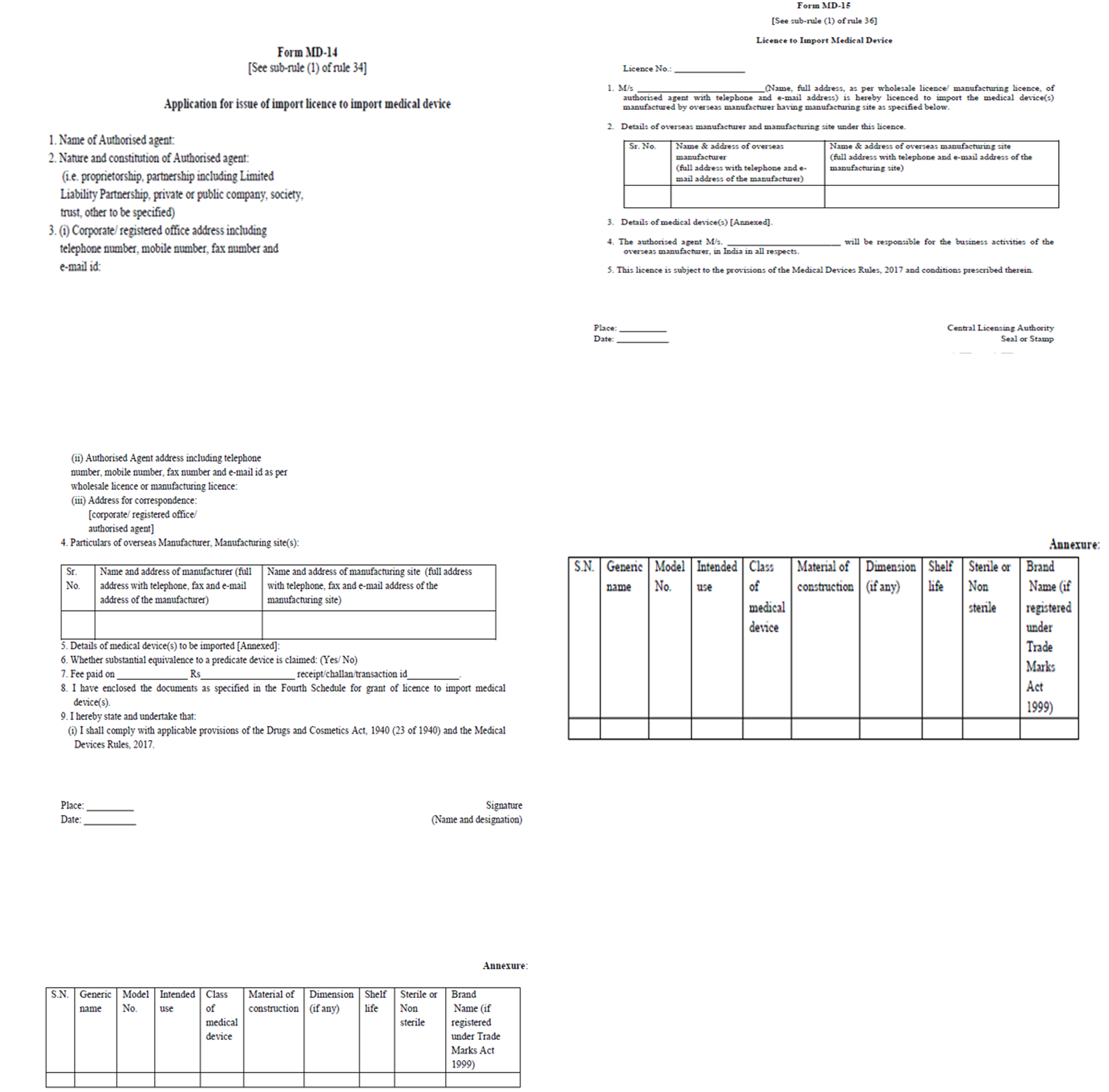
자료: 중앙의약품표준통제국(CDSCO)
신청 절차 관할 기관
중앙의약품표준통제국(CDSCO)의 산하기관 CLA(Central Licensing Authority)에서 모든 의료기기 수입 절차의 관할 기관으로서의 역할 수행 중이다.(연락처·전화: +91-11-23236973, Email: dci@nic.in)
시사점
인도 의료기기 시장은 2025년까지 250억~300억 달러 규모로 성장할 것으로 예상된다. 하지만 인도 내 제조업체들의 낮은 기술력으로 인해 의료기기 산업의 75%를 수입에 의존하고 있다. 이에 인도 정부는 의료기기 수입절차를 간소화하고 신속하게 진행하기 위해 법적 제도를 마련하고 있으며, 이에 대한 이해는 인도 의료기기 시장에 진출하려는 한국 기업들에 중요할 것으로 판단된다.
자료: 중앙의약품표준통제국(CDSCO), KOTRA 뭄바이 무역관 자료 종합
<저작권자 : ⓒ KOTRA & KOTRA 해외시장뉴스>

KOTRA의 저작물인 (인도 의료기기 인증 및 등록 절차)의 경우 ‘공공누리 제4 유형: 출처표시+상업적 이용금지+변경금지’ 조건에 따라 이용할 수 있습니다. 다만, 사진, 이미지의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다.
-
1
대인도 의료기기 수출 관련 규제 및 물품 인증절차
인도 2018-12-28
-
2
코로나19가 쏘아올린 변화, 인도 원격의료시장
인도 2020-07-24
-
3
인도의 자가 진단 키트 시장 동향
인도 2020-07-16
-
4
인도 화장품 인증 및 등록 절차
인도 2020-05-07
-
5
코로나19 경제위기를 대응하기 위한 인도 정부의 움직임
인도 2020-05-28
-
6
2021년 인도 의약품 산업 정보
인도 2022-01-20
-
1
2023년 인도 전기자동차 산업 정보와 현지 동향
인도 2023-12-12
-
2
2022년 인도 반도체산업 정보
인도 2022-10-20
-
3
2022 인도 완구산업 정보
인도 2022-08-05
-
4
2022년 인도 화장품 산업 정보
인도 2022-05-25
-
5
2021년 인도 철강산업 정보
인도 2022-01-20
-
6
2021년 인도 보안산업 정보
인도 2022-01-20













